La batería en el automóvil:
El término » batería « designa una interconexión entre varias células galvánicas que se usan como fuente de energía. Pero también una célula galvánica individual se denomina vulgarmente » batería”.
Las células galvánicas transforman la energía química almacenada en ellas directamente en energía eléctrica.
Se diferencia entre baterías recargables y no recargables. La diferencia consiste en que en las baterías recargables (acumuladores), las reacciones durante la descarga pueden invertirse y la batería puede recargarse y descargarse. De este modo es posible una transformación múltiple de la energía química en eléctrica y a la inversa.
Las células galvánicas sirven como fuentes de tensión continua.
La combinación de los materiales de los electrodos dan nombre a la célula galvánica, por ejemplo, célula de níquel metal híbrido.
Dependiendo de si la célula se carga o descarga, cambia la composición del electrólito, así como el material de los electrodos. La clase de material con que se fabrican los electrodos depende de la tensión nominal de la célula.
Por medio de una conexión paralela de las células galvánicas se aumenta la capacidad de la batería. La tensión de la batería es siempre igual.
Si es necesaria una tensión superior a la de las células, éstas pueden conectarse en serie. La tensión total de la batería corresponde a la suma de las células individuales. En el ejemplo siguiente, la tensión total es Uges = U1 + U2 + U3.
Si la tensión y/o la capacidad de la célula para el caso de aplicación no son suficientes, pueden conectarse varias células en serie o en paralelo.
Conexión de las células en serie y en paralelo







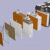

Los comentarios están cerrados